MENU
芳香族アミン(アニリン)の構造・製法・性質・反応
目次
はじめに
【プロ講師解説】このページでは『芳香族アミン(アニリン)の構造・製法・性質・反応』について解説しています。
芳香族アミンとは
- ベンゼン環にアミノ基(-NH2)が置換した化合物を芳香族アミンという。
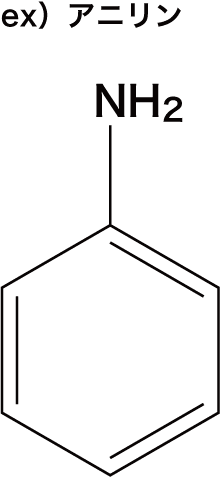
- 高校化学で出てくる芳香族アミンのほとんどはアニリンであるため、今回はアニリンに特化して解説する。
アニリンの製法
- アニリンはニトロベンゼンやアニリン塩酸塩を介して次のような流れでつくられる。
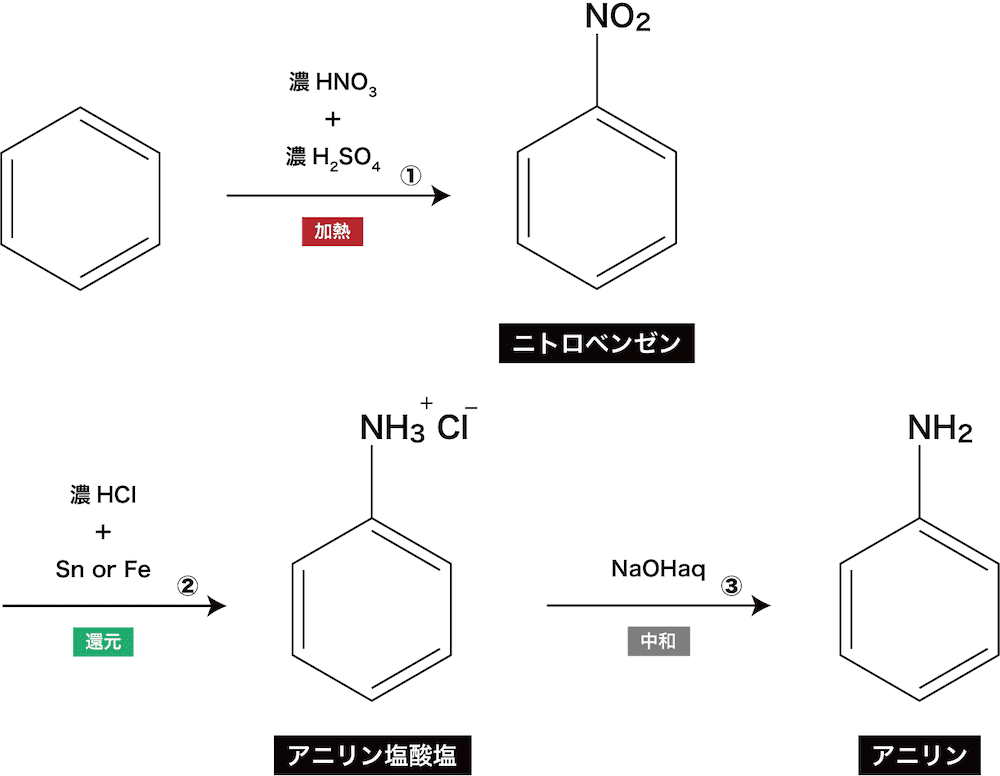
- ベンゼンに混酸(濃硝酸+濃硫酸)を加えることでニトロベンゼンを得る。
- ニトロベンゼンに酸性条件下(アニリンは酸化されやすいので強い酸化力をもたない塩酸をよく用いる)で還元剤である金属スズSn(or鉄Fe)を加え、アニリン塩酸塩を得る。
- アニリン塩酸塩に水酸化ナトリウム水溶液を加え、アニリンを得る。この反応は弱塩基遊離反応である。
アニリンの反応①(塩基としての反応)
- アニリンはアミノ基(-NH2)をもつため、弱塩基性物質である。
- したがって、酸性物質と酸塩基反応(中和反応)を起こしたり、強塩基性物質と弱塩基遊離反応を起こしたりする。
※中和反応について詳しくは中和(定義・塩・中和反応式の作り方など)を参照
※弱塩基遊離反応について詳しくは【弱酸・弱塩基遊離反応】原理や公式、反応式の作り方などを参照
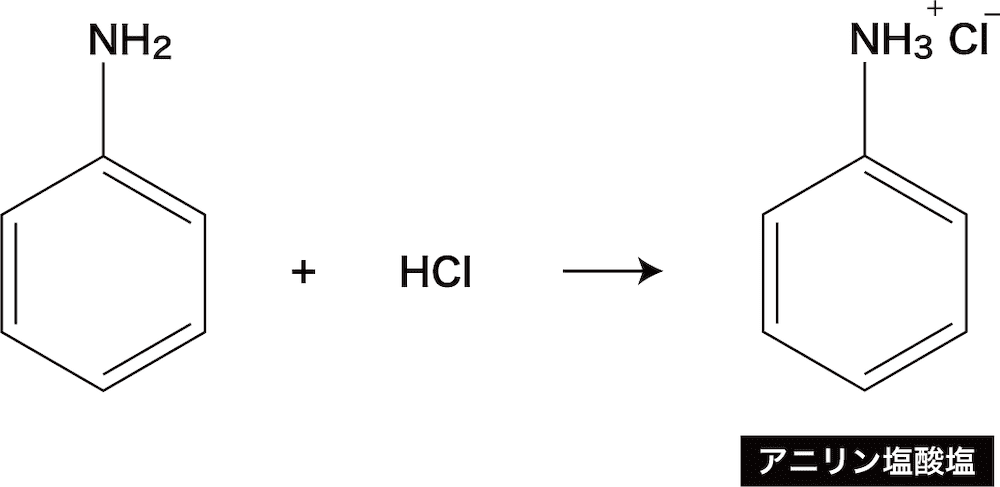
アニリンと塩酸の酸塩基反応
- アニリンは塩酸HClと酸塩基反応を起こしアニリン塩酸塩を生じる。
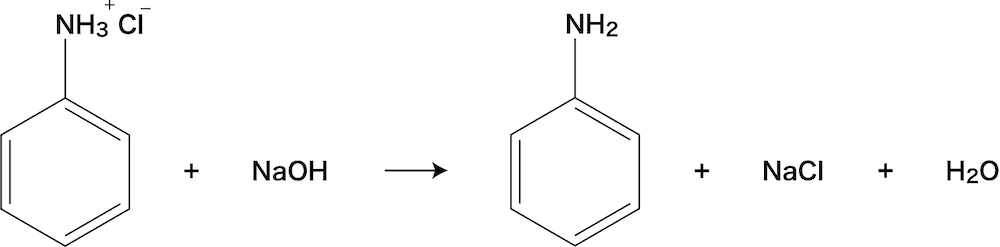
アニリン塩酸塩と水酸化ナトリウムの弱塩基遊離反応
- 上で生成したアニリン塩酸塩を強塩基であるNaOHと反応させると、弱塩基であるアニリンが遊離する。
アニリンの反応②(アセチル化)
- アニリンを無水酢酸(CH3CO)2Oと反応させるとアセトアニリドが生成する。
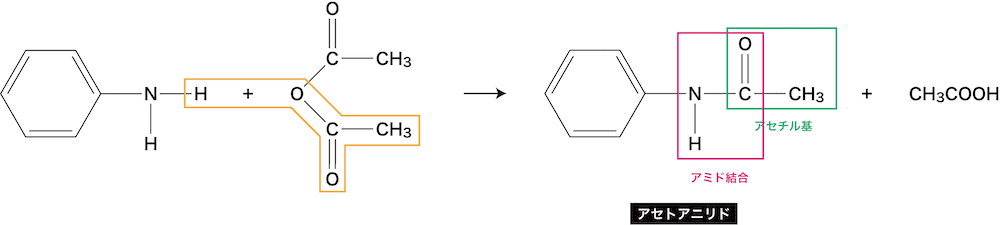
- この反応はアミノ基(-NH2)の検出反応として用いられている。
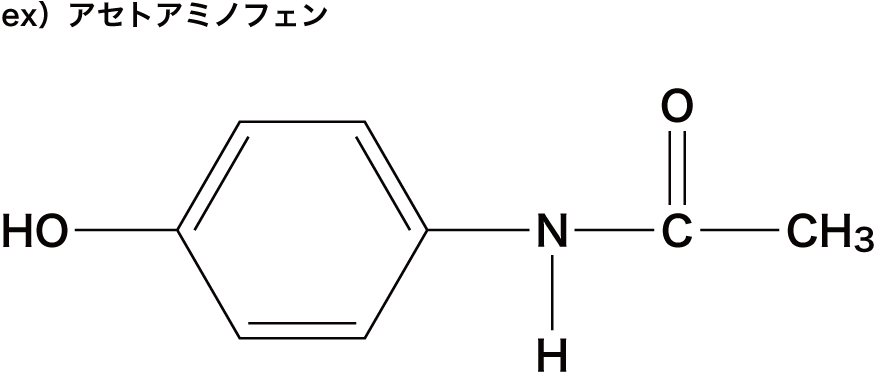
- また、アセトアニリドは白色の結晶でかつて解熱鎮痛剤として用いられていた。しかし、副作用(溶血作用)をもつため現在はあまり使用されておらず、アセトアミノフェンなどで代用されている。
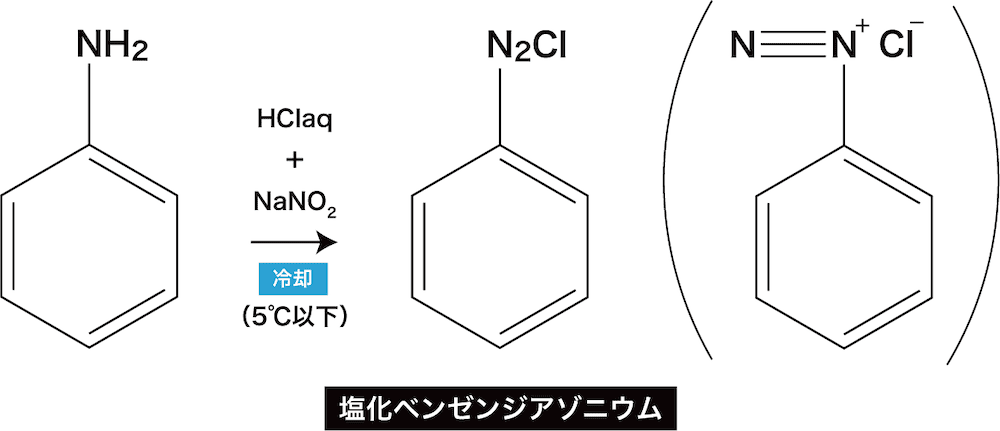
アニリンの反応③(ジアゾ化)
- アニリンに希塩酸HClと亜硝酸ナトリウムNaNO2を加えて5℃以下に保ったまま反応させると、ジアゾ基(-N+≡N)をもつ塩化ベンゼンジアゾニウムが生成する。この反応をアニリンのジアゾ化という。
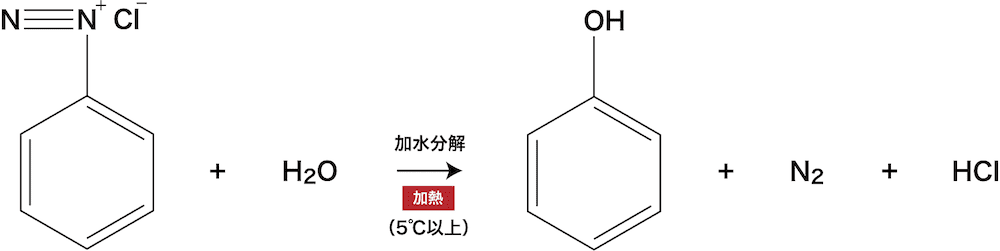
- このとき生成したジアゾニウム塩は不安定であるため、5℃以上に加熱すると分解してしまいN2の発生とともにフェノールが生成する。
アニリンの反応④(ジアゾカップリング)
- 温度を5℃以下の低温に保ったまま塩化ベンゼンジアゾニウムにNaOHaqを加えて塩基性にし、(フェノール由来の)ナトリウムフェノキシドと反応させるとジアゾカップリングとよばれる反応が起こる。

- このとき生成したp-ヒドロキシアゾベンゼンは赤橙色をしており合成染料として用いられる。
アニリンの反応⑤(検出反応)
- アニリンの検出反応として知っておくべきは次の2つである。
●アニリンの検出反応
- さらし粉を加えると紫色を呈する
- 二クロム酸カリウムを加えると黒色沈殿を生じる
- アニリンにさらし粉CaCl(ClO)・H2O水溶液を加えると紫色になる。
- また、アニリンにニクロム酸カリウムK2Cr2O7を加えるとアニリンブラックとよばれる黒色沈殿が生じる。