MENU
有機化合物(芳香族)の分離法〜仕組みや実験手順などを解説〜
目次
はじめに
【プロ講師解説】このページでは『有機化合物(芳香族)の分離法〜仕組みや実験手順などを解説〜』について解説しています。
抽出とは
- 混ざり合わない2つの溶媒(水とジエチルエーテルなど)を用いると、芳香族化合物を分離することができ、この操作を抽出という。
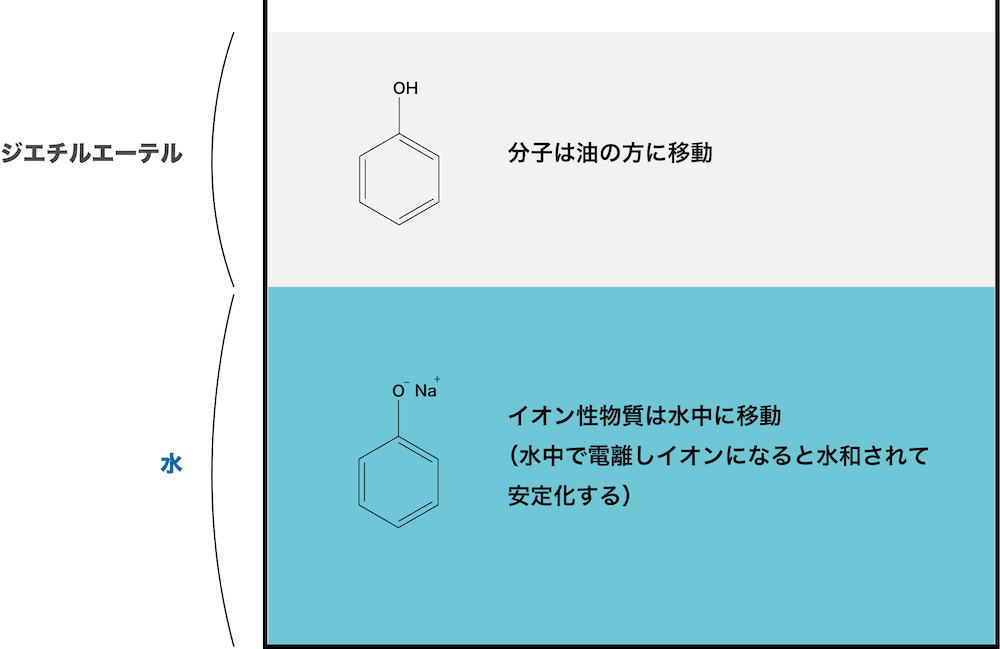
- 芳香族化合物のほとんどは極性の高い水よりも極性の低いジエチルエーテルのような有機溶媒に溶けやすい。
- しかし、芳香族化合物でも、酸・塩基反応によって“塩”に変えられると水の方によく溶けるようになる。
- ちなみに、ジエチルエーテルと水の密度を比較するとジエチルエーテルの方が小さいので、上層がジエチルエーテル層、下層が水層になっている点も把握しておこう。
分離の原理
- ここからは芳香族化合物の分離の原理について、酸性物質であるフェノールと安息香酸、塩基性物質であるアニリンを使って解説する。
アニリン
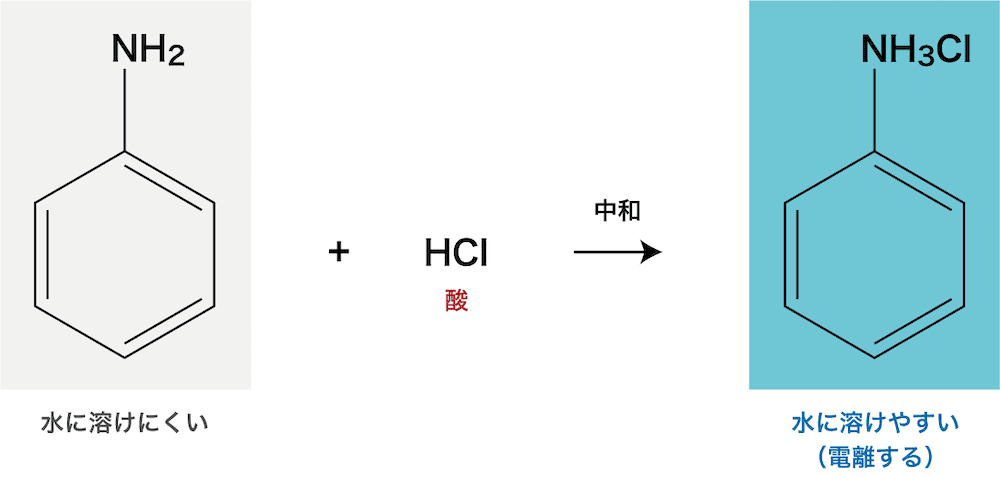
- アニリンを含む有機溶媒に塩酸を加えると、中和反応が起きてアニリンがアニリン塩酸塩となり、水層へ移動する。
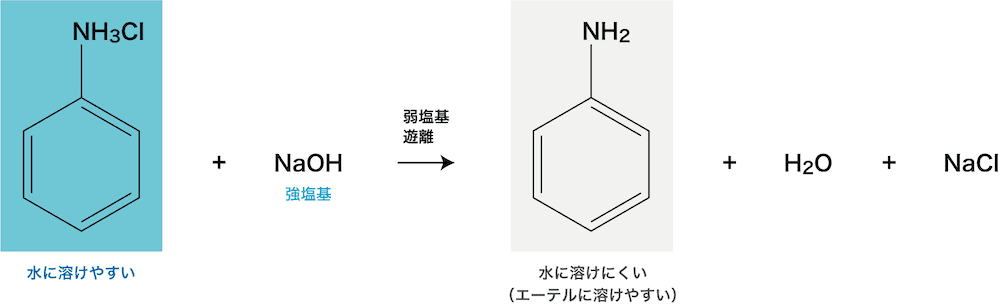
- 次に、強塩基である水酸化ナトリウム水溶液を加えると、弱塩基のアニリンが遊離して(弱塩基遊離反応)再び有機溶媒層へと移動する。
フェノール・安息香酸
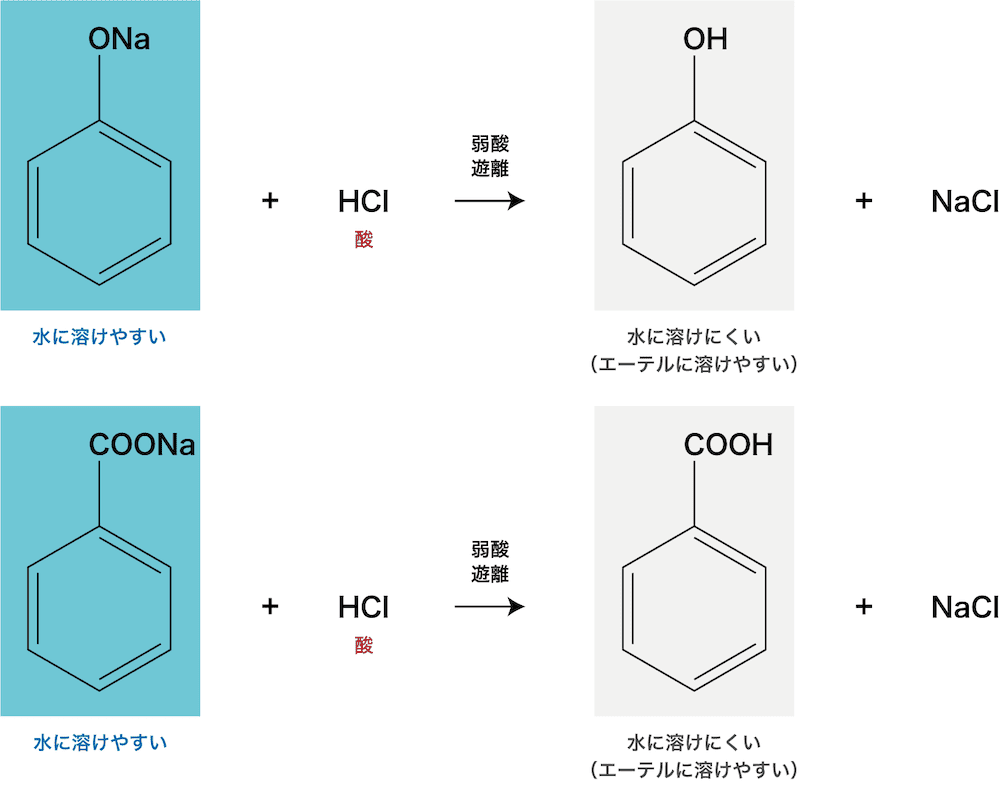
- フェノールと安息香酸はともに酸性物質なので、水酸化ナトリウム水溶液を加えると中和されて塩となり、水層へと移動する。

- 次に、強酸である塩酸を加えると、弱酸であるフェノールや安息香酸が遊離して再び有機溶媒層へと移動する。
- ここからはフェノールと安息香酸をどのように分離していくかという点について考える。
- フェノール類(名称・製法・性質・反応など)にあるように、炭酸はカルボン酸よりも弱く、フェノールよりも強い酸である。これを利用する。
- フェノールと安息香酸のエーテル溶媒に炭酸水素ナトリウム水溶液を加えると、(弱酸遊離反応により)安息香酸だけが反応して水によく溶ける塩となり、水層へと移動する。
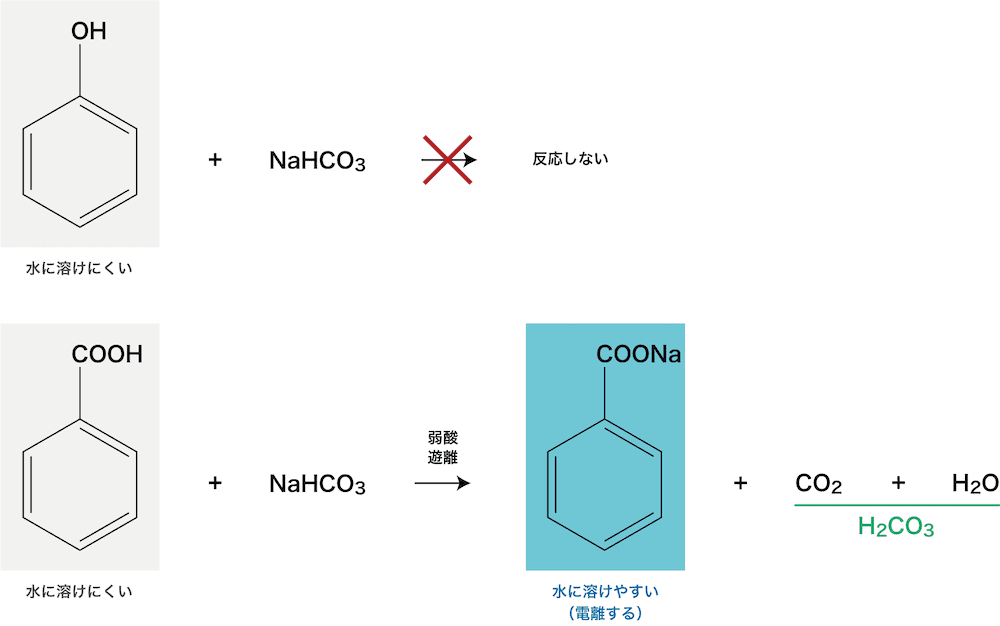
- また、安息香酸ナトリウムとナトリウムフェノキシドの混合水溶液に二酸化炭素を通じると、フェノールが遊離して、有機溶媒層へ移動する。
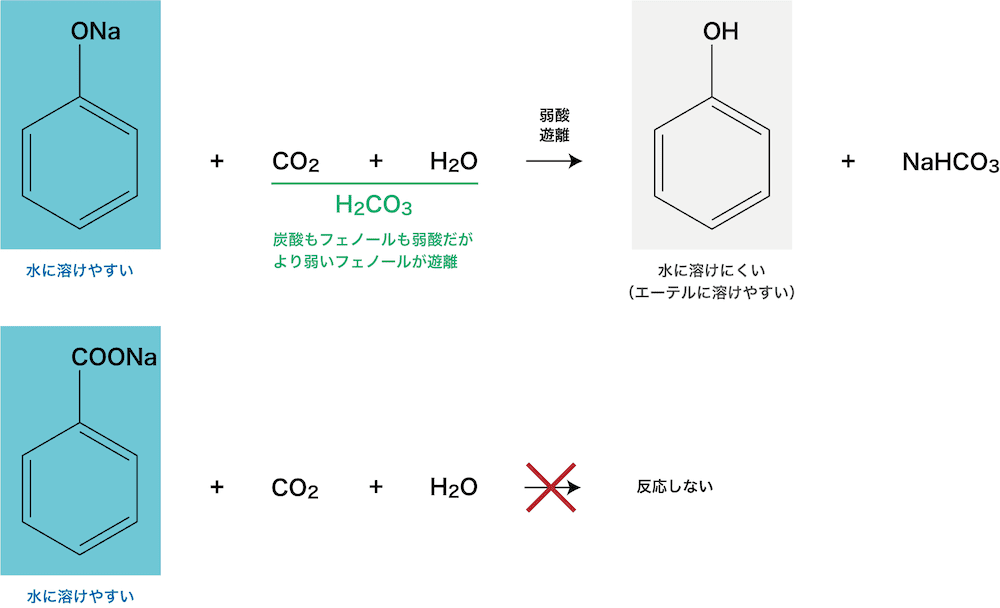
- これらの反応を利用して、フェノール・安息香酸・アニリン・ベンゼンの混合液からそれぞれの物質を分離すると次のようになる(分離には分液ろうとを使用)。
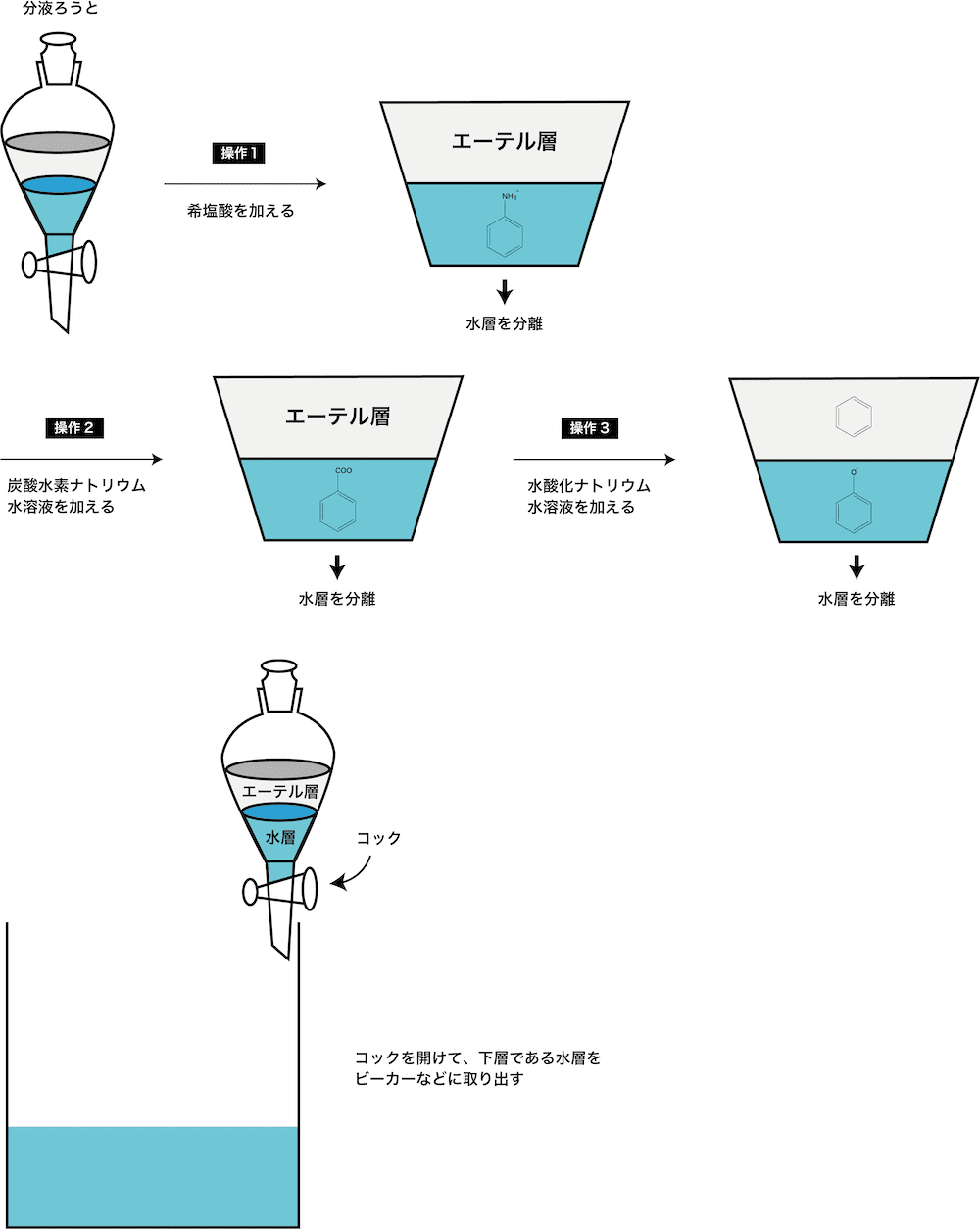
【操作1】塩酸を加えると塩基性物質であるアニリンのみがイオン形になり水層へと移動する
→水層を分離することでアニリンGET!!
【操作2】炭酸水素ナトリウム水溶液を加えると弱酸遊離反応により安息香酸のみがイオン形になり水層へと移動する
→水層を分離することで安息香酸GET!!
【操作3】水酸化ナトリウム水溶液を加えるとフェノールがナトリウムフェノキシド(フェノキシドイオン)となり水層へと移動する
→水層を分離することでフェノールGET!!
※ベンゼンは中性物質であり、①②③の全てで反応しないので最後までエーテル層に残る。
分液ろうとは大学で有機化学系の実験を行うときに使用します。
溶液を混ぜたときに二酸化炭素などの気体が発生すると、分液ろうと内の圧力が上がって液が漏れてくる恐れがあるため、(栓が閉まっていることを確認した上で)定期的に分液ろうとを逆さまにしてコックを抜き、ガス抜きをする必要があります。














