MENU
【鉄メッキ】ブリキとトタン(違い・イオン化傾向に基づく錆びやすさの理由など)
目次
はじめに
【プロ講師解説】このページでは『【鉄メッキ】ブリキとトタン(違い・イオン化傾向に基づく錆びやすさの理由など)』について解説しています。
鉄の腐食
- 鉄板に水が付着すると、鉄Feは鉄(Ⅱ)イオンとなり、水に移行する(鉄板が溶ける)。
\[ \mathrm{Fe→Fe^{2+}+2e^{-}} \]
- また、空気中から水に溶けた酸素O2がFeの放出した電子eーを受け取り、水酸化物イオンOHーとなる。
\[ \mathrm{O_{2}+4e^{-}+2H_{2}O→4OH^{-}}(還元反応) \]
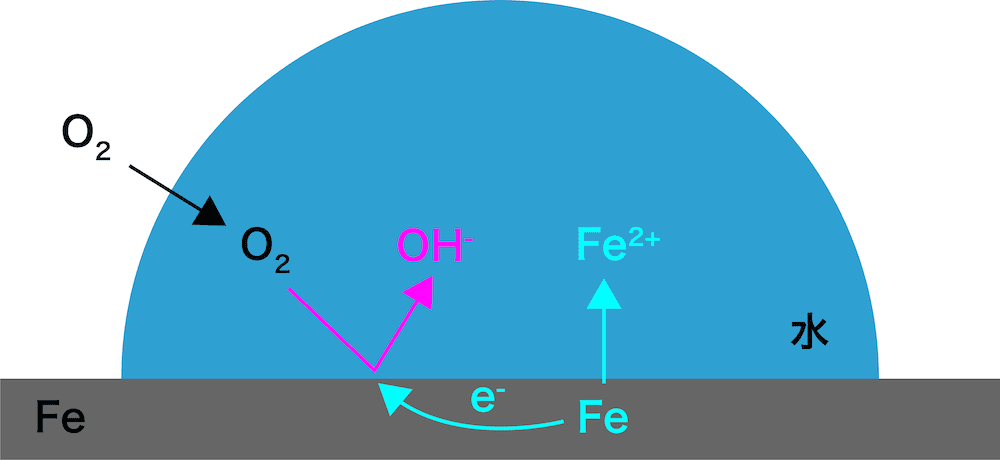
- この酸化還元反応が鉄板上で連続して起こることで、腐食が進む。
- ちなみに、上記2つの半反応式を足し合わせると、酸化還元反応全体の反応式を導くことができる。
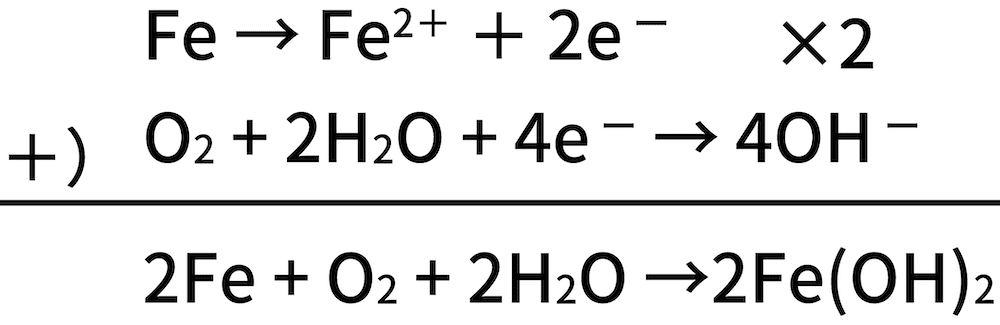
参考:半反応式・酸化還元反応式(作り方・覚え方・問題演習など)
- 生成物のFe(OH)2は非常に酸化されやすいため、すぐに酸化鉄(Ⅲ)Fe2O3などを生じる。Fe2O3は鉄の赤さびの主成分である。
鉄メッキの分類
- 鉄の表面を加工する(メッキを施す)ことで、鉄の腐食を防ぐことができる。
- 代表的な鉄メッキとして、トタンとブリキが存在する。
| 鉄メッキ | 解説 | 例 |
|---|---|---|
| トタン | 鉄の表面に亜鉛メッキを施したもの | 屋根など |
| ブリキ | 鉄の表面にスズメッキを施したもの | おもちゃ・缶詰など |
- 鉄メッキのうち、トタンは鉄の表面を亜鉛Znで覆ったもので、鉄板でつくられた屋根の加工などに用いられる。
- 一方、ブリキは鉄の表面をスズSnで覆ったもので、鉄でつくられたおもちゃや缶詰の加工などに用いられる。
トタンメッキの仕組み
- トタンは鉄Feの表面を亜鉛Znで覆ったものである。

- トタンは主に”トタン屋根”として用いられているので、(外の雨風に晒され)傷がつくことが多い。

- 傷ついた部分に雨水などの水滴が付くと、次の反応が起こる。
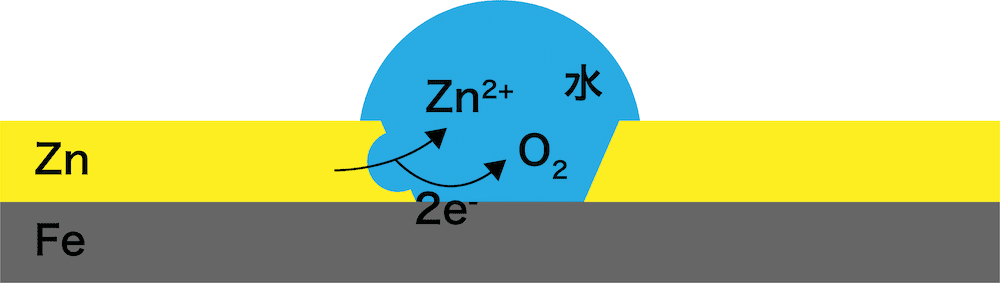
- FeとZnのイオン化傾向を比較すると、Znの方が大きい。
- したがって、Znが優先的に溶け出して亜鉛イオンZn2+となる。
\[ \mathrm{Zn→Zn^{2+}+2e^{-}} \]
- その結果、Feがイオンになって溶ける(=腐食する)のを防ぐことができる。
ブリキメッキの仕組み
- ブリキは鉄Feの表面をスズSnで覆ったものである。

- ブリキに傷がついたとする。

- ここに水滴が付くと、次の反応が起こる。
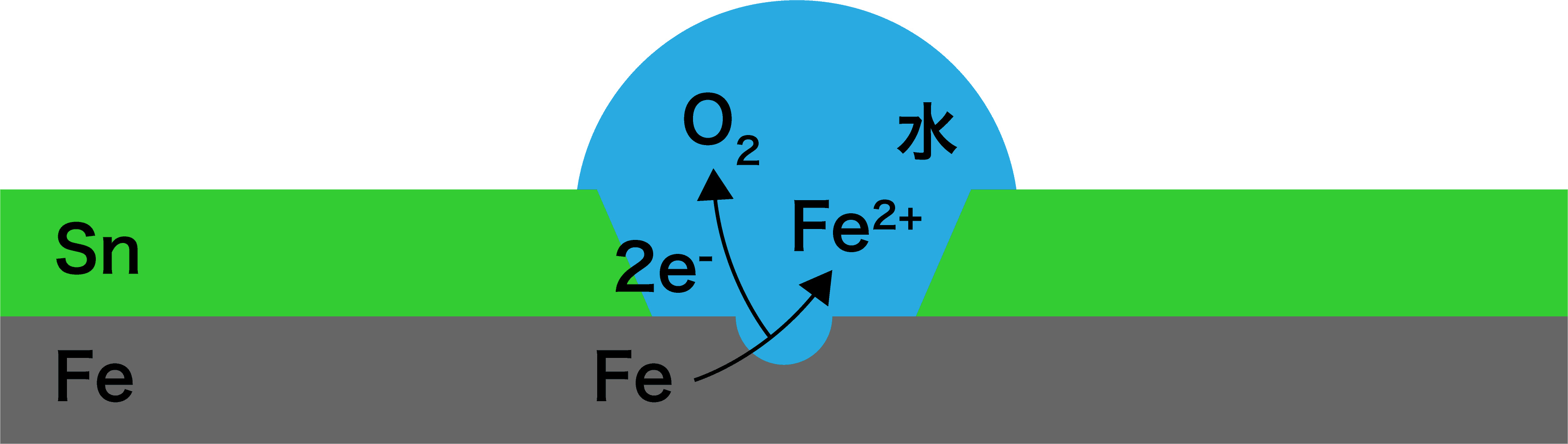
- SnとFeのイオン化傾向を比較すると、Feの方が大きい。
- したがって、Feが優先的に溶け出して鉄(Ⅱ)イオンFe2+となる。
\[ \mathrm{Fe→Fe^{2+}+2e^{-}} \]
- 「Feの方が先に溶けてしまうんじゃ意味がないのでは」と考える人がいるかもしれないが、Snはトタンで使われているZnよりもイオン化傾向が小さいため、傷がついていない状態では水がついても溶けにくく、丈夫である。
- したがって、傷がつく危険性が低いもの(おもちゃ・缶詰など)においては、ブリキが用いられることが多い。
トタンとブリキまとめ
- トタンとブリキの特徴についてまとめる。
| トタン | ブリキ | |
|---|---|---|
| メッキ | 亜鉛 | スズ |
| 通常時の強度 | 弱い | 強い |
| 傷がつき水が付着したとき | Znが溶ける (=鉄が錆びにくい) | Feが溶ける (=鉄が錆びやすい) |
| 用途 | 屋根 | おもちゃ・缶詰 |














