MENU
水和物(水和物を含む物質)の加熱
目次
はじめに
【プロ講師解説】このページでは『水和物(水和物を含む物質)の加熱』について解説しています。
水和物を含む物質の加熱
- 結晶中において一定の割合で含まれている水は水和水(結晶水)とよばれる。
- 硫酸銅(Ⅱ)水溶液を冷却して得られる結晶は、硫酸銅(Ⅱ)CuSO4:水和水H2O=1:5の物質量比からなる。この結晶を硫酸銅(Ⅱ)五水和物といい、化学式は次の通りである。
\[ \mathrm{CuSO_{4}・5H_{2}O} \]
- 硫酸銅(Ⅱ)五水和物の構造は次のようになっている。
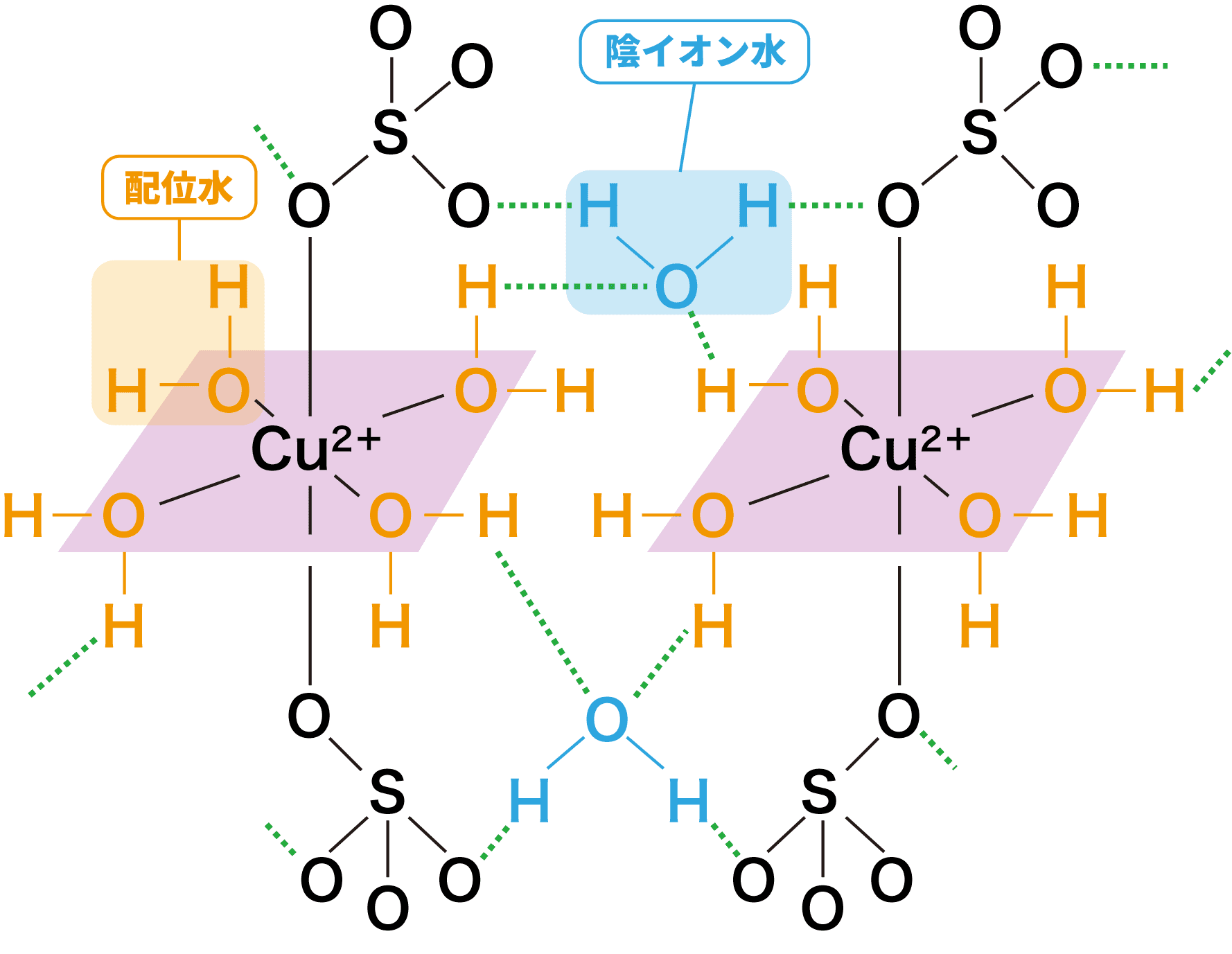
- 硫酸銅(Ⅱ)五水和物CuSO4・5H2Oは青色結晶であり、これを加熱すると水和水が徐々に取れていき、最終的には白色結晶である(無水)硫酸銅(Ⅱ)CuSO4となる。
- このときの質量変化は次のようになる。
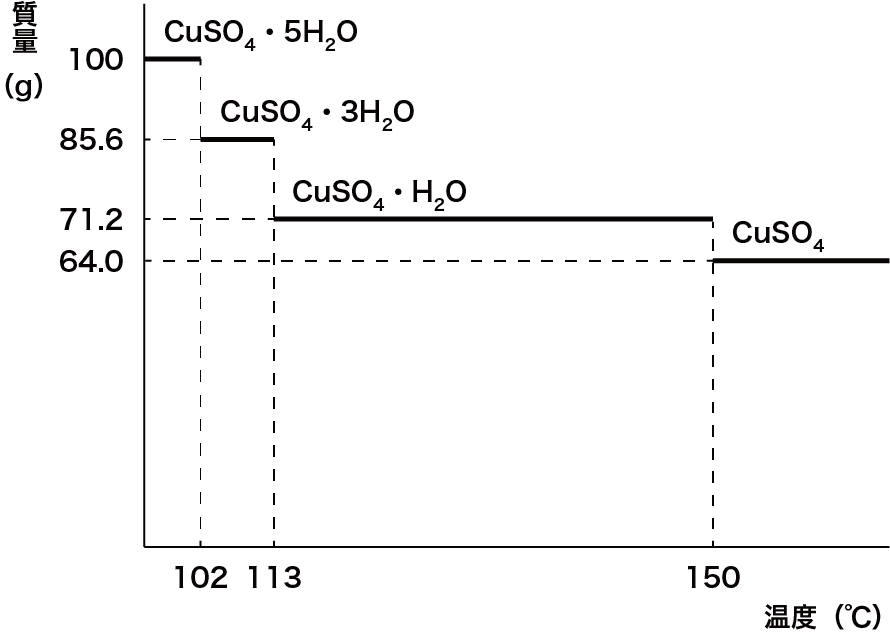
- 水和水が減るにつれて質量が減少しているのが確認できる。なお、硫酸銅(Ⅱ)五水和物の質量変化を使った計算問題は入試頻出なので次のページで確認しておこう。
- このように、水和水を含む物質を加熱すると、一般に水和水が外へ出ていく変化が起こり、シュウ酸カルシウム一水和物などでも同様である。(シュウ酸カルシウム一水和物の場合水和水が取れた後も熱分解反応が進む)















