MENU
分子結晶(例・特徴・融点・電気伝導性・柔らかい理由など)
はじめに
【プロ講師解説】このページでは『分子結晶(例・特徴・融点・電気伝導性・柔らかい理由など)』について解説しています。
分子結晶とは
- ドライアイスCO2・ヨウ素I2・氷H2Oなど、多数の分子が分子間力によって引き合って、規則正しく配列してできた結晶を分子結晶という。
参考:分子間力(水素結合・ファンデルワールス力・沸点のグラフなど)
分子間力には方向性がありません。したがって、分子結晶は、方向性のある共有結合によってできる共有結合結晶より、密度の高い構造になることが多いです。
ドライアイスの分子結晶
- 二酸化炭素CO2分子が分子間力で規則正しく配列してできた白色の結晶をドライアイスという。
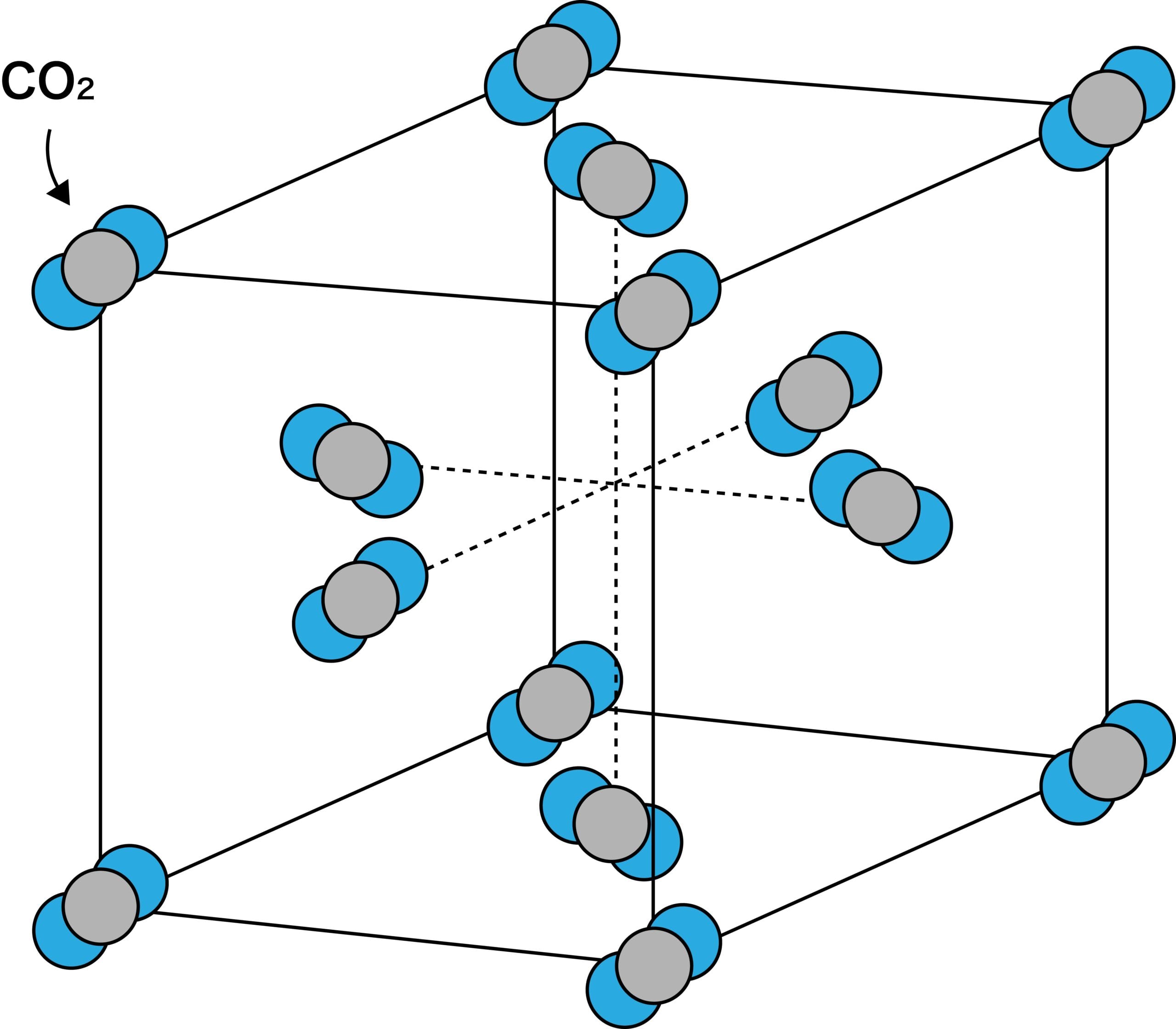
- ドライアイスは常温で容易に昇華(固体↔︎気体)する。昇華については次のページを参照のこと。
ヨウ素の分子結晶
- ヨウ素I2分子が分子間力で規則正しく配列すると黒紫色の結晶になる。
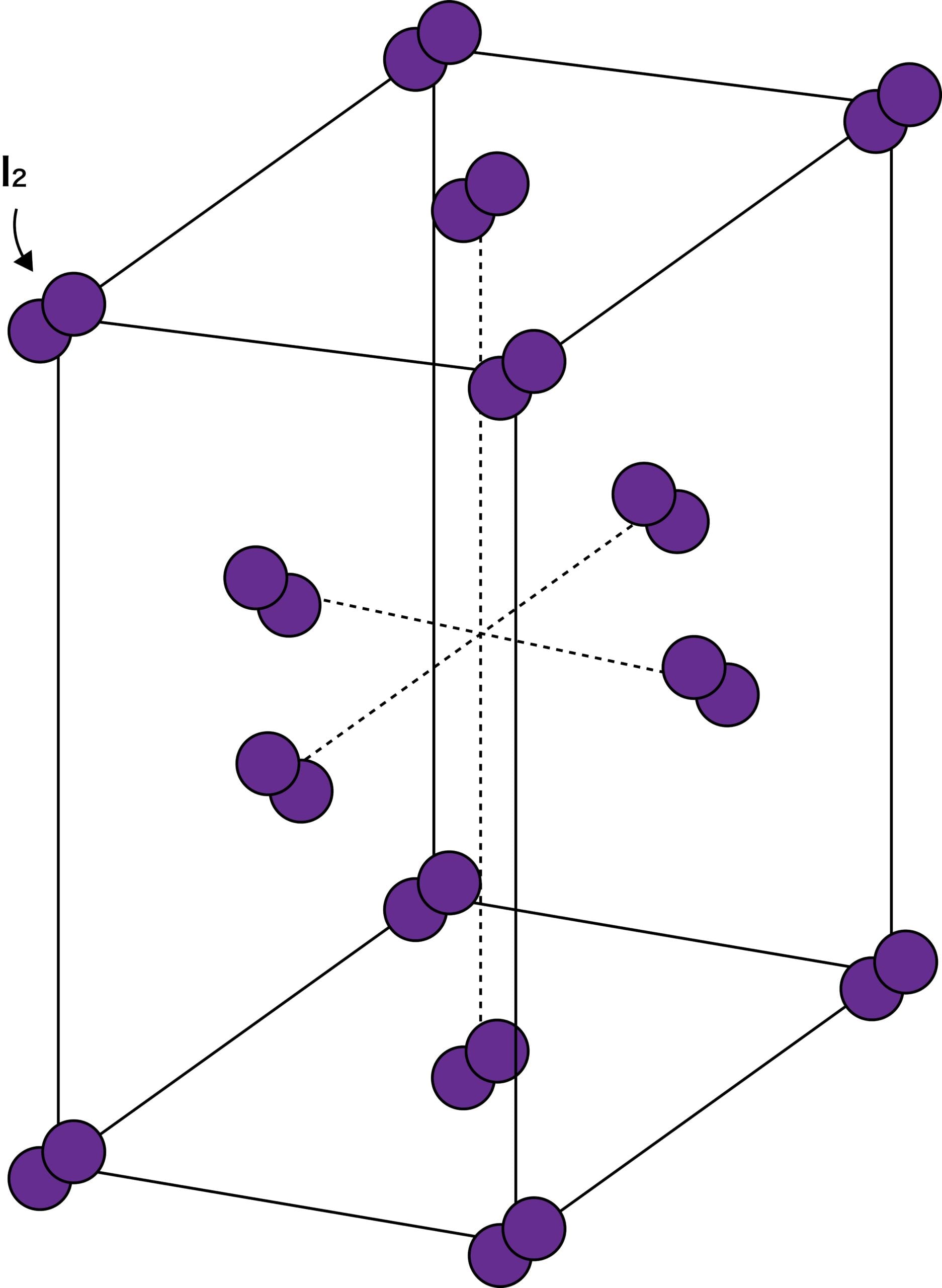
- ヨウ素は穏やかに加熱を行うことで昇華する。
分子結晶の性質
- 分子結晶には次のような特徴がある。
●分子結晶の特徴
- 電気伝導性がない
- 融点が低い
- 昇華性をもつ
- 柔らかい
❶ 電気伝導性がない
- 分子結晶は電気的に中性な分子によりできているため、電気伝導性がない。
❷ 融点が低い
- 分子結晶は比較的弱い結合である分子間力によってできている。したがって、結合が切れることによる状態変化が起こりやすく、融点が低い。
参考:分子間力(水素結合・ファンデルワールス力・沸点のグラフなど)
❸ 昇華性をもつ
- 分子結晶は状態変化が起こりやすいため、昇華性(固体↔︎気体変化を起こす性質)をもつ。
- 昇華については次のページを参照のこと。
参照:【物質の三態】状態変化とは?原理や用語(凝縮・昇華等)を図を使って解説!
❹ 柔らかい
- 分子結晶は分子間力によってできているため、共有結合結晶などと比較して柔らかく、外力によって壊れやすい。
分子結晶まとめ
この『分子結晶(例・特徴・融点・電気伝導性・柔らかい理由など)』のページで解説した内容をまとめる。
- ドライアイスCO2・ヨウ素I2・氷H2Oなど、多数の分子が分子間力によって引き合って、規則正しく配列してできた結晶を分子結晶という。
- 分子結晶には次のような特徴がある。
❶ 電気伝導性がない
❷ 融点が低い
❸ 昇華性をもつ
❹ 柔らかい
演習問題
【プロ講師解説】化学のグルメでは、高校化学・化学基礎の一問一答問題を公開しています。問題一覧は【スマホで出来る】一問一答(高校化学・化学基礎)でご覧下さい。
ドライアイスCO2・ヨウ素I2・氷H2Oなど、多数の分子が分子間力によって引き合って、規則正しく配列してできた結晶を【1】という。
解答/解説:タップで表示
解答:【1】分子結晶
ドライアイスCO2・ヨウ素I2・氷H2Oなど、多数の分子が分子間力によって引き合って、規則正しく配列してできた結晶を分子結晶という。
CO2分子が分子間力で規則正しく配列してできた白色の結晶が【1】である。常温で容易に【2(固体→気体)】する。
解答/解説:タップで表示
解答:【1】ドライアイス【2】昇華
CO2分子が分子間力で規則正しく配列してできた白色の結晶がドライアイスである。常温で容易に昇華する。
I2分子が分子間力で規則正しく配列すると【1】色の結晶ができる。穏やかに加熱を行うことで【2(固体→気体)】する。
解答/解説:タップで表示
解答:【1】黒紫【2】昇華
I2分子が分子間力で規則正しく配列すると黒紫色の結晶ができる。穏やかに加熱を行うことで昇華する。
分子結晶は電気伝導性が【1(ある or ない)】。
解答/解説:タップで表示
解答:【1】ない
分子結晶は電気的に中性な分子によりできているため、電気伝導性がない。
分子結晶は融点が【1(高 or 低)】い。
解答/解説:タップで表示
解答:【1】低
分子結晶は比較的弱い結合である分子間力によってできている。したがって、結合が切れることによる状態変化が起こりやすく、融点が低い。
分子結晶は共有結合結晶と比較して【1(硬or柔らか)】い。