MENU
気体の拡散と混合
目次
はじめに
【プロ講師解説】このページでは『気体の拡散と混合』について解説しています。
熱とは
- どんな粒子も温度に応じた運動をしていて、これを熱運動という。温度が高くなると熱運動のエネルギーが大きくなり、熱運動が激しくなる。
- 粒子の熱運動は、煙の広がりを考えると理解しやすい。煙が部屋のある一箇所で発生すると、時間とともに部屋中に広がっていく。これは、粒子が熱運動で広がっていくためであり、この現象を拡散という。
- 水素H2と二酸化炭素CO2を別々の集気ビンに入れ、ガラス板を挟んで口を重ねた結果、ガラス板を取り除くと次のようになる。
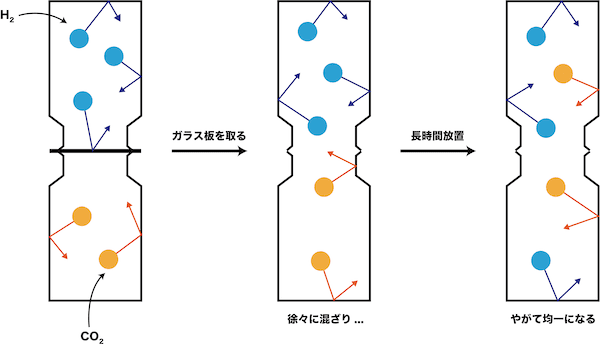
- 混合時に反応しないとすれば、両者の物質量n1、n2を足し合わせて、混合気体の物質量nとすることができる。
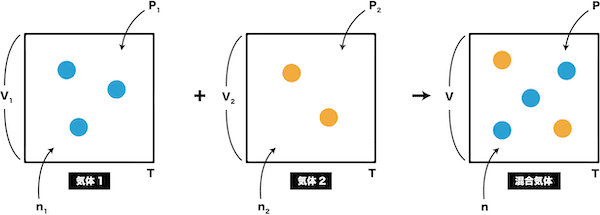
\[ \mathrm{n_{1}+n_{2}=n・・・①} \]
- 気体の状態方程式PV=nRTより、①式は次のように変形することができる。
\[ \begin{align}&n_{1}+n_{2}=n\\
&\Leftrightarrow\frac{ P_{1}V_{1} }{ RT_{1} }+\frac{ P_{2}V_{2} }{ RT_{2} }=\frac{ PV }{ RT }\\
&\Leftrightarrow \frac{ P_{1}V_{1} }{ T_{1} }+\frac{ P_{2}V_{2} }{ T_{2} }=\frac{ PV }{ T }・・・② \end{align}\]
- nのように、PV/Tの和を取ることもできる。さらに一定の量があると、②式は次のように変形できる。
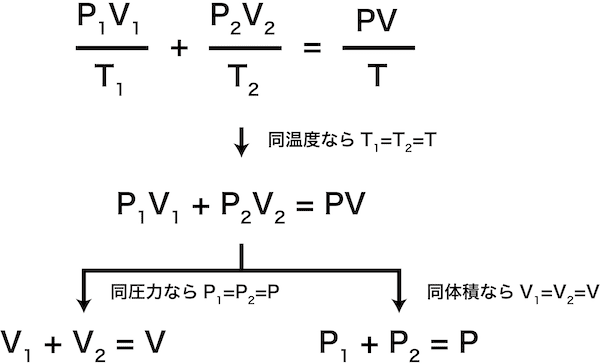
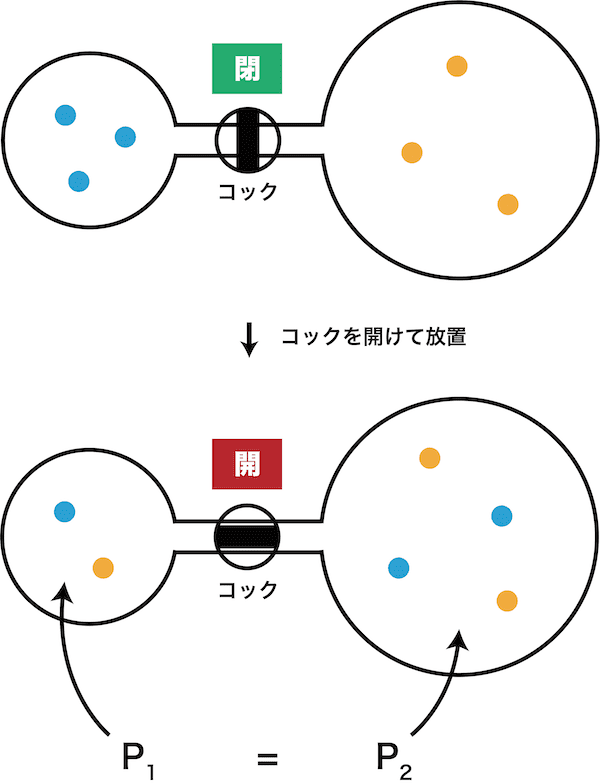
- コックでつないだ次の容器の場合は、気体の拡散によって最終的に左右の圧力が等しくなる。また、気体の体積は容積に一致する。