MENU
活性化エネルギー・反応熱【高校化学・化学基礎一問一答】
問1
分子同士が衝突して化学反応が起こるとき、エネルギーの高い状態(【1】)を経由する。物質を【1】にするために必要な最低限のエネルギーを【2】という。
解答/解説:タップで表示
解答:【1】活性化状態【2】活性化エネルギー
●活性化エネルギー
反応物質が反応するために必要なエネルギー
●活性化状態
活性化エネルギーを得て反応途中の段階にある、非常に不安定な状態
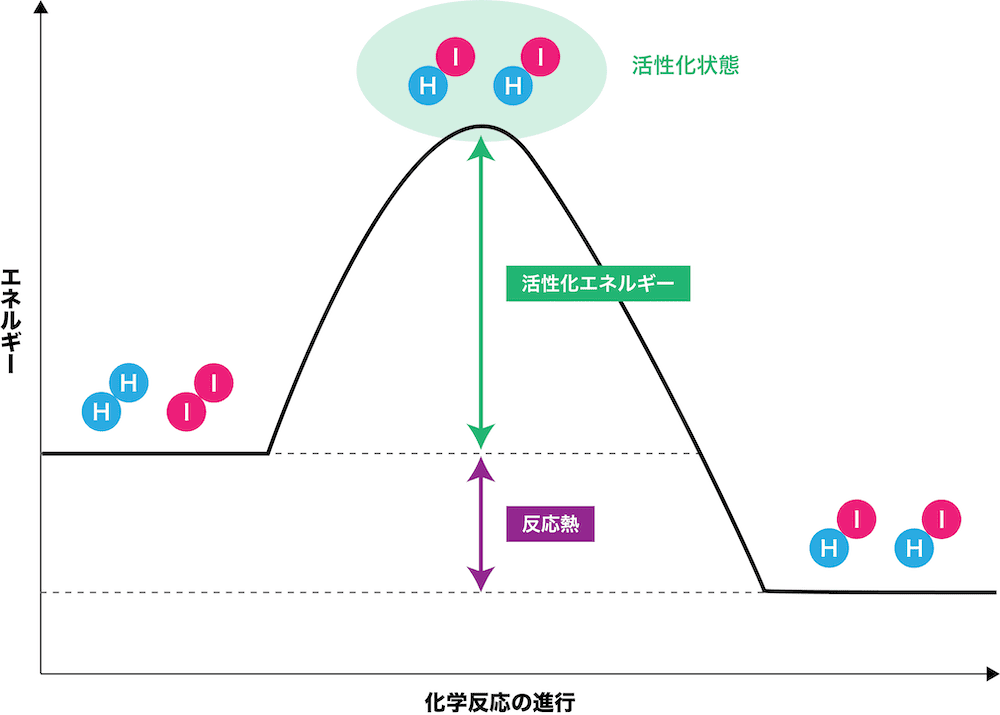
参考:活性化エネルギーと反応熱
問2
活性化エネルギーが小さいほど、反応速度は【1(速 or 遅)】くなる。
解答/解説:タップで表示
解答:【1】速
活性化エネルギーが大きい場合
活性化エネルギーは「反応物が活性化状態になるために必要なエネルギー」である。したがって、これが大きいということは「反応物が活性化状態になるまで時間がかかる」ということになる。すると当然、反応全体にかかる時間も長くなる。

活性化エネルギーが小さい場合
活性化エネルギーが小さい場合、「反応物が活性化状態になるまでにかかる時間が短い」ので、反応全体にかかる時間も短くなる。
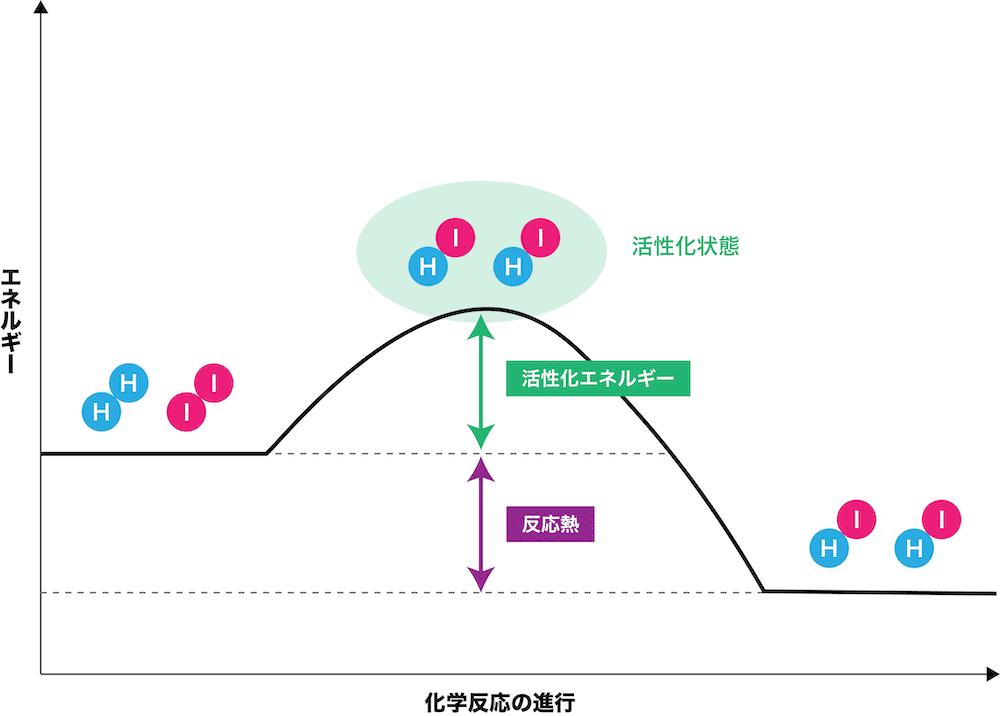
参考:活性化エネルギーと反応熱
問3
反応物のエネルギーと生成物のエネルギーの差を【1】という。














