MENU
シュバイツァー試薬や二硫化炭素を用いてセルロースを溶かす方法
目次
はじめに
【プロ講師解説】このページでは『シュバイツァー試薬や二硫化炭素を用いてセルロースを溶かす方法』について解説しています。
セルロースを溶かす方法
- セルロースを溶かす方法には『シュバイツァー試薬を用いる方法』と『水酸化ナトリウムと二硫化炭素を用いる方法』が存在する。
シュバイツァー試薬を用いる方法
- シュバイツァー試薬はアンモニア性水酸化銅(Ⅱ)溶液である。
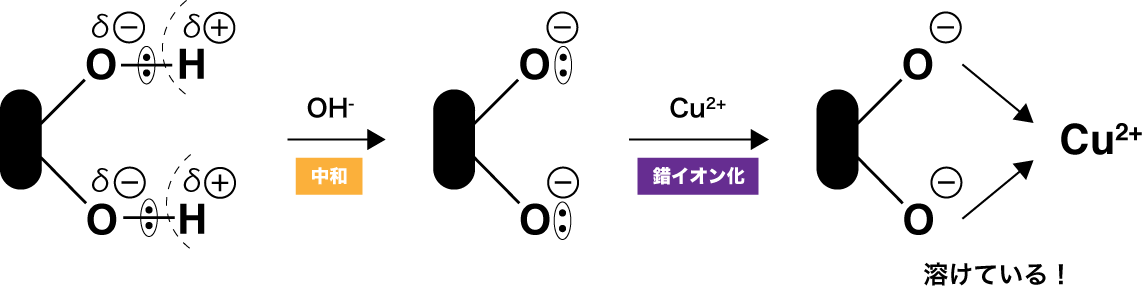
- セルロースのヒドロキシ基は僅かに電離してH+を出し、酸の役割を果たしている。
\[ \mathrm{R-O-H⇆R-O^{-}+H^{+} }\]
- シュバイツァー試薬に含まれる遷移金属イオンであるCu2+は、錯イオンをつくりやすい性質がある。
- したがって、セルロースの-Oーと配位結合して錯イオンを形成し、セルロースが溶解する。
水酸化ナトリウムと二硫化炭素を用いる方法
- セルロースを濃NaOH水溶液に入れると、半透明のアルカリセルロースとなる。
- これに適切な処理を施したのち、ニ硫化炭素(CS2)を加えると、黄〜黄赤色のゼリー状物質(セルロースキサントゲン酸ナトリウム)が得られる。
- これを希NaOH水溶液に溶かすと、透明感のある赤褐色で粘性をもつコロイド溶液(ビスコース)となる(セルロースは溶けた!)。














