MENU
見かけの分子量(平均分子量)
はじめに
【プロ講師解説】このページでは『見かけの分子量(平均分子量)』について解説しています。
見かけの分子量とは
- 混合気体は2種類以上の気体が混ざったものである。
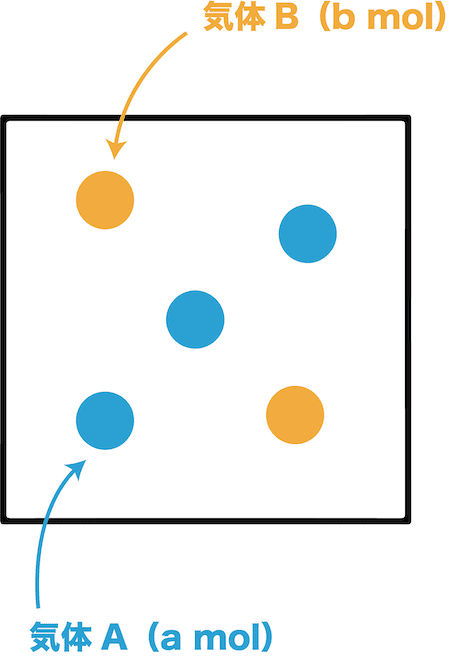
- したがって、混合気体の分子量を考えるときは(これと決まった分子量がないため)少し工夫をする必要がある。
\[ M_{全}=
\underbrace{ M_{A}×\frac{ n_{A} }{ n_{A}+n_{B} } }
_{ \text{ 気体A }}
+
\underbrace{ M_{B}×\frac{ n_{B} }{ n_{A}+n_{B} } }
_{ \text{ 気体B }} \]
- 混合気体の分子量は、各気体の分子量に各気体のモル分率を掛けたものを足し合わせることで求めることができる(混合気体そのものの分子量というのは定められていないため、各元素の分子量を使って「見かけ上(計算上)」の値を算出するイメージ)。
- 混合気体の分子量は計算で求めた理論上の値のため、見かけの分子量(平均分子量)とよばれる。
演習問題
化学のグルメでは、高校化学・化学基礎の一問一答問題を公開しています。問題一覧は【スマホで出来る】一問一答(高校化学・化学基礎)でご覧下さい。
混合気体の分子量を考えるときは、各気体の分子量に各気体のモル分率を掛けたものを足し合わせる。こうして求めた理論上の分子量を【1】という。
解答/解説:タップで表示
解答:【1】平均分子量(見かけの分子量)
\[ M_{全}=
\underbrace{ M_{A}×\frac{ n_{A} }{ n_{A}+n_{B} } }
_{ \text{ 気体A }}
+
\underbrace{ M_{B}×\frac{ n_{B} }{ n_{A}+n_{B} } }
_{ \text{ 気体B }} \]
混合気体の分子量は、各気体の分子量に各気体のモル分率を掛けたものを足し合わせることで求めることができる(混合気体そのものの分子量というのは定められていないため、各元素の分子量を使って「見かけ上(計算上)」の値を算出するイメージ)。
混合気体の分子量は計算で求めた理論上の値のため、見かけの分子量(平均分子量)とよばれる。
27℃で8.3Lの容器にN2が0.80mol、O2が0.20mol入っている。次の問いに答えよ(気体定数R=8.3×103とする)。
(1)容器内の圧力(Pa)を求めよ。
(2)混合気体の平均分子量(見かけの分子量)を求めよ。
解答/解説:タップで表示
解答:(1)3.0×105Pa(2)29
(1)気体の状態方程式を用いて、容器内の圧力(Pa)を求める。
\[ \begin{align} PV&=nRT\\
P&=\frac{ nRT }{ V }\\
&=\frac{ 1.0×8.3×10^{3}×(27+273) }{ 8.3 }\\
&=3.0×10^{5}\mathrm{(Pa)} \end{align} \]
(2)先ほどの公式を用いる。
\[ \begin{align}&M_{全}=
\underbrace{ M_{A}×\frac{ n_{A} }{ n_{A}+n_{B} } }
_{ \text{ 気体A }}
+
\underbrace{ M_{B}×\frac{ n_{B} }{ n_{A}+n_{B} } }
_{ \text{ 気体B }}\\
&=28×\frac{ 0.80 }{ 0.80+0.20 }+32×\frac{ 0.20 }{ 0.80+0.20 }\\
&=22.4+6.4\\
&=28.8 \end{align} \]














