固体の溶解度【高校化学・化学基礎一問一答】
問1
物質にはそれぞれ100gの水に溶けることのできる限界の量が決まっており、その量を【1】という。
また、【1】まで溶質を溶かした溶液を【2】溶液という。
解答/解説:タップで表示
解答:【1】溶解度【2】飽和
物質にはそれぞれ100gの水に溶けることのできる限界の量(=固体の溶け残りが発生しないギリギリの量)が決まっており、その量を溶解度という。
溶解度まで溶質を溶かした溶液を飽和溶液という。
参考:固体の溶解度(温度との関係・計算問題・溶解度曲線など)
問2
固体の溶解度は【1】に依存して変化する。【1】による溶解度の変化をグラフで表したものを【2】という。
解答/解説:タップで表示
解答:【1】温度【2】溶解度曲線
固体の溶解度は、温度に依存して変化する。(基本的に温度が高くなるほどよく溶けるようになる)
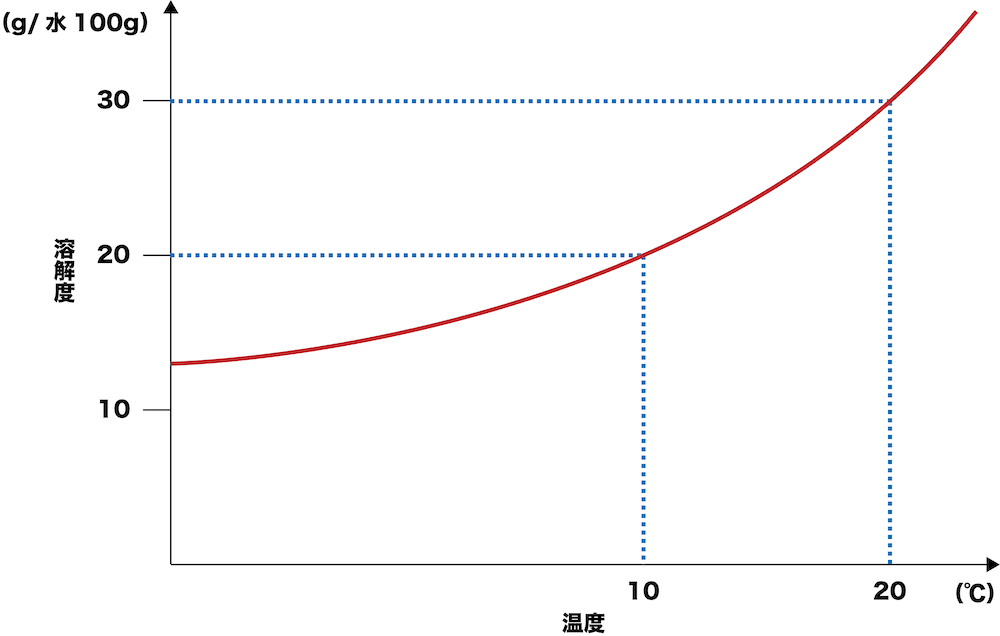
温度による溶解度の変化をグラフで表したものを溶解度曲線という。

参考:固体の溶解度(温度との関係・計算問題・溶解度曲線など)
問3
物質が溶解している水溶液の条件(主に温度)に変化を加え、目的の物質を固体として析出する操作を【1】という。
高校化学・化学基礎の計算問題が苦手な人に向けた計算ドリルを発売しました。豊富な問題数で、入試頻出の計算問題の解き方を身につけることができます。

無機化学の知識を総ざらいできるオリジナル問題集ができました。解答・解説編には入試頻出事項が一通りまとめられており、まとめノート/参考書としての役割も果たします。

有機化学に関する入試頻出事項を演習することのできるオリジナル問題集が紙の本になりました。暗記項目だけではなく、計算問題や思考力が問われる問題についても触れています。

元講師、薬剤師、イラストレーター
数百名の中高生向け指導経験あり(過去生徒合格実績:東工大・東北大・筑波大・千葉大・岡山大・早稲田大・慶應義塾大・東京理科大・上智大・明治大など)。
2014年よりwebメディア『化学のグルメ』を運営
公式オンラインストアで販売中の理論化学ドリルシリーズ・有機化学ドリル等を執筆