MENU
鉄の工業的製法(手順・反応式・銑鉄・スラグ・鋼など)
はじめに
【プロ講師解説】このページでは『鉄の工業的製法(手順・反応式・銑鉄・スラグ・鋼など)』について解説しています。
鉄の工業的製法
- 鉄Feの工業的製法は次の手順で考える。
●STEP1
溶鉱炉で鉄鉱石(主成分:Fe2O3)・コークスC・石灰石CaCO3に熱風を吹き込み、銑鉄を得る。
●STEP2
転炉で融解した銑鉄に酸素O2を吹き込み、鋼を得る。
まず、溶鉱炉(高炉)に鉄鉱石(主成分:Fe2O3)・コークスC・石灰石CaCO3を入れ、熱風を吹き込む。
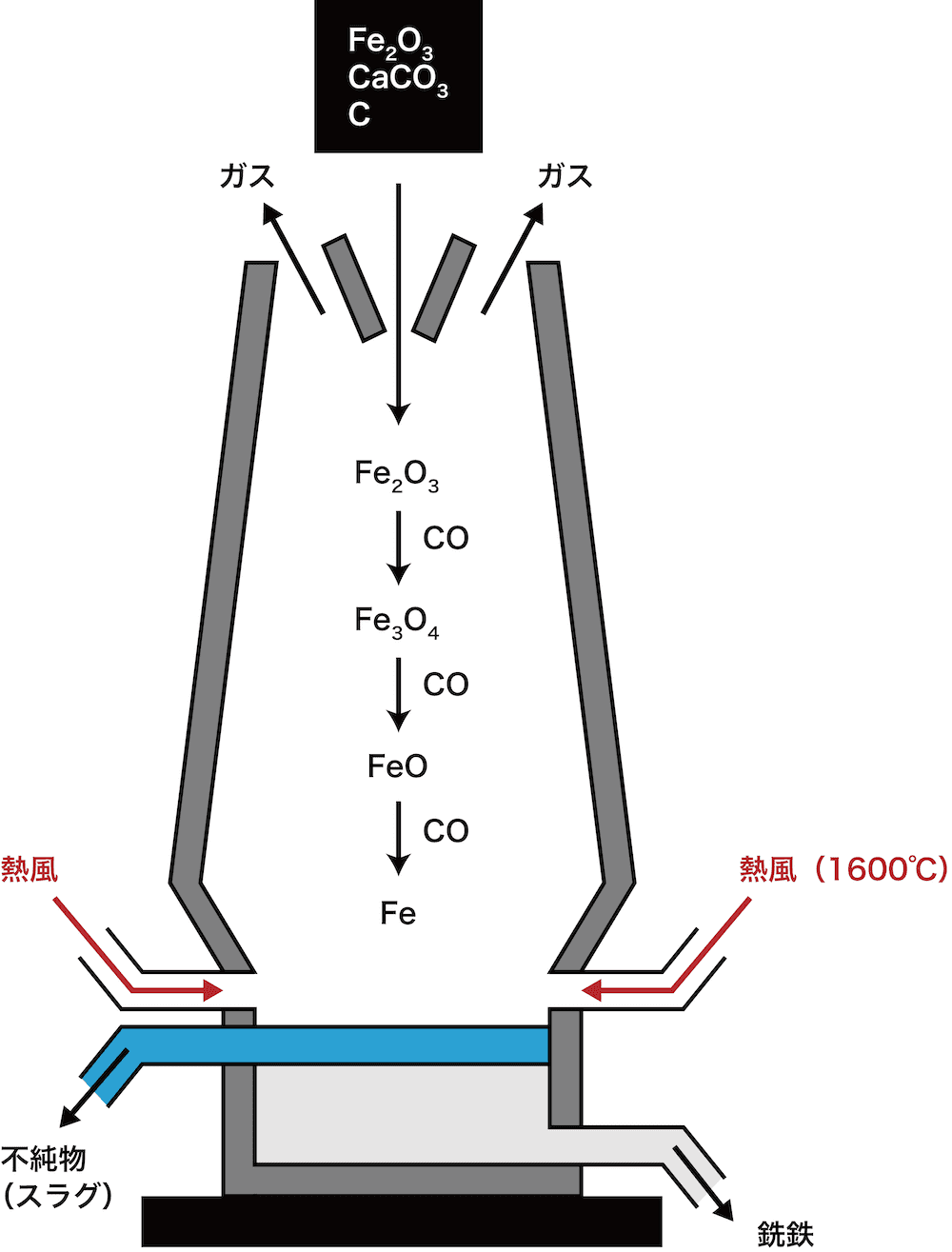
熱風によりCaCO3の熱分解及びCの燃焼が起こり、二酸化炭素CO2が生じる。
\[ \begin{align}&\mathrm{CaCO_{3}→CaO+CO_{2}}\\
&\mathrm{C+O_{2}→CO_{2}} \end{align}\]
このCO2をコークスの存在下で加熱すると、一酸化炭素COになる。
\[ \mathrm{C+CO_{2}→2CO} \]
COにより、Fe2O3が段階的に還元されて銑鉄(Fe)となる。
\[ \begin{align}&\mathrm{3Fe_{2}O_{3}+CO→2Fe_{3}O_{4}+CO_{2}}\\
&\mathrm{Fe_{3}O_{4}+CO→3FeO+CO_{2}}\\
&\mathrm{FeO+CO→Fe+CO_{2}} \end{align}\]
ちなみに、STEP1の全体の反応式は次の通りである。
\[ \mathrm{Fe_{2}O_{3}+3CO→2Fe+3CO_{2}} \]
銑鉄は炭素を多く含み(C>2%)、硬くてもろいという性質がある。
なお、不純物として鉄鉱石に含まれていたSiO2やAl2O3は、石灰石の熱分解で生じたCaOと反応し、CaSiO3やCa(AlO2)2に変化する。これをスラグという。
次に、転炉で融解した銑鉄に酸素O2を吹き込むことで鋼を得る。
鋼は(銑鉄と異なり)炭素をほとんど含んでおらず(0.02%<C<2%)、粘り気があって硬いという性質をもつ。
間接還元と直接還元
- 先述のように、鉄鉱石(主成分:Fe2O3)を、コークスCから生じる一酸化炭素COにより還元することを間接還元という。
- 一方、鉄鉱石の一部は高温のコークスCに触れて直接的に還元される。これを直接還元という。
\[ \mathrm{Fe_{2}O_{3}+3C→2Fe+3CO} \]
水素還元
- 近年、鉄の工業的製法として水素還元という技術が注目されている。
- 水素還元では、溶鉱炉(高炉)に鉄鉱石(主成分:Fe2O3)をいれ、これを水素により還元する。
\[ \mathrm{Fe_{2}O_{3}+3H_{2}→2Fe+3H_{2}O} \]
- 先述の通り、コークスCを使った鉄鉱石の還元では二酸化炭素CO2が生じる。水素還元ではCO2の代わりにH2Oが生じるため、 CO2排出量を抑えることができ、環境への影響を軽減できる可能性がある。














