MENU
冷却曲線(グラフの見方や凝固点降下との関係、溶質で傾く理由など)
目次
はじめに
【プロ講師解説】このページでは『冷却曲線(グラフの見方や凝固点降下との関係、溶質で傾く理由など)』について解説しています。
冷却のグラフ
- 冷却時間と温度の関係をグラフで表すと次のようになる。

- 冷却開始直後であるA-B間は全て気体の状態である。
- 凝固点(気体が液体に変わる温度)であるBに達すると気体が液体に変わり始め、Cで完全に液体になる。(ちなみにB-C間で温度が下がらないのは気体から液体への“状態変化”により発熱しているから)
- C-D間は全て液体、D-E間は液体が徐々に固体になっており、E以降は全て固体の状態である。
冷却曲線とは
- 上のグラフのうち、液体から固体に変化する部分を切り取ってみよう。

- このグラフを冷却曲線という。
- 冷却曲線の見方は次の通りである。
●冷却曲線の見方
①a〜b間は液体である
②b〜c間はまだ液体である
※凝固点で凝固せず、液体のまま冷却されることを過冷却という
③c〜e間は固体と液体が共存している
※c点で結晶核(結晶のもとになるもの)ができ、一気に固体(結晶)ができる(c〜d間)
※このとき温度が急激に上昇しているのは凝固熱が発生しているからである
※c〜dで固体ができたものの、まだ全てが固体になったわけではなく、残りの液体はd〜eの間で凝固し固体となる。
※d〜eの間で温度が一定なのは凝固によって発生する熱と冷却によって奪われる熱が等しいためである
④e以降は完全に固体である
溶質を入れたときの冷却曲線
- 上で見てきた冷却曲線は「水(溶媒)のみ」のものだったが、それに溶質を加えて“溶液”になった場合、冷却曲線はどのように変化するのかを確認する。
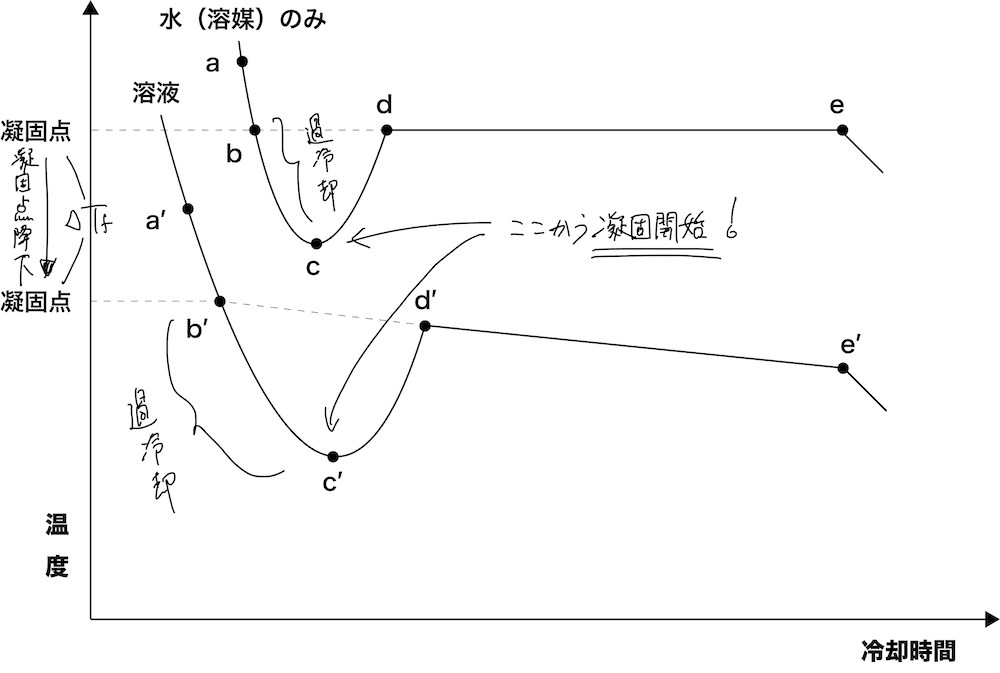
- 基本的には溶媒のみのときと同じ形をしているが、d′-e′間が右下がりになっているということに注意しよう。
- これは、溶液の凝固では、溶媒だけが先に凝固していくため、溶液の濃度が増加した結果、溶液の凝固点が降下して液温が下がっていることを示している。














