MENU
陽イオン交換樹脂・陰イオン交換樹脂(作り方・原理・反応式など)
目次
はじめに
【プロ講師解説】このページでは『陽イオン交換樹脂・陰イオン交換樹脂(作り方・原理・反応式など)』について解説しています。
イオン交換樹脂とは
- イオンを含む溶液にある物質を触れさせておくと、その物質中のイオンと溶液中のイオンが入れ替わる。この現象をイオン交換という。また、このような作用を行う物質をイオン交換樹脂という。
イオン交換樹脂の作り方
- スチレンに少量のp-ジビニルベンゼンを混ぜて共重合させ、立体網目状構造の樹脂を作成する。
- さらに、ベンゼン環に置換基を導入し、直径が1mm程度のビーズ状に加工すると、イオン交換樹脂をつくることができる。
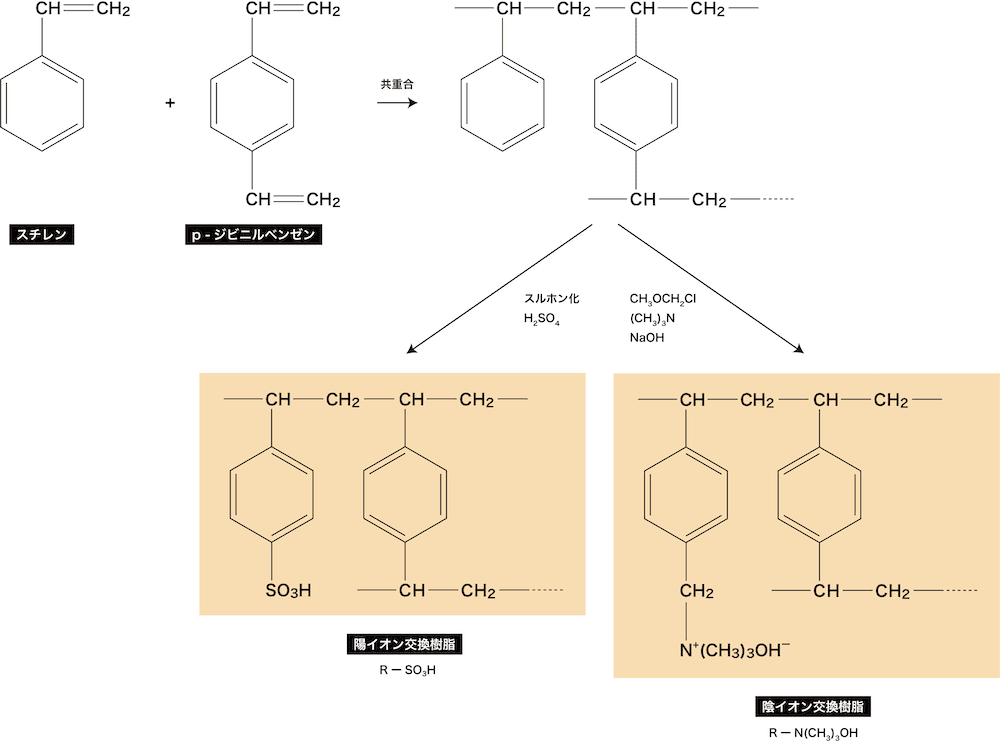
イオン交換樹脂の仕組み
- 陽イオン交換樹脂、陰イオン交換樹脂の原理について解説する。
陽イオン交換樹脂
- カラムとよばれる円筒形の管に陽イオン交換樹脂(R-SO3ーH+)を詰め、そこに上から塩化ナトリウムNaCl水溶液を流す。
- その結果、水溶液中のNa+は陽イオン交換樹脂中のH+と置き換わって、下から塩酸HClが出てくる。

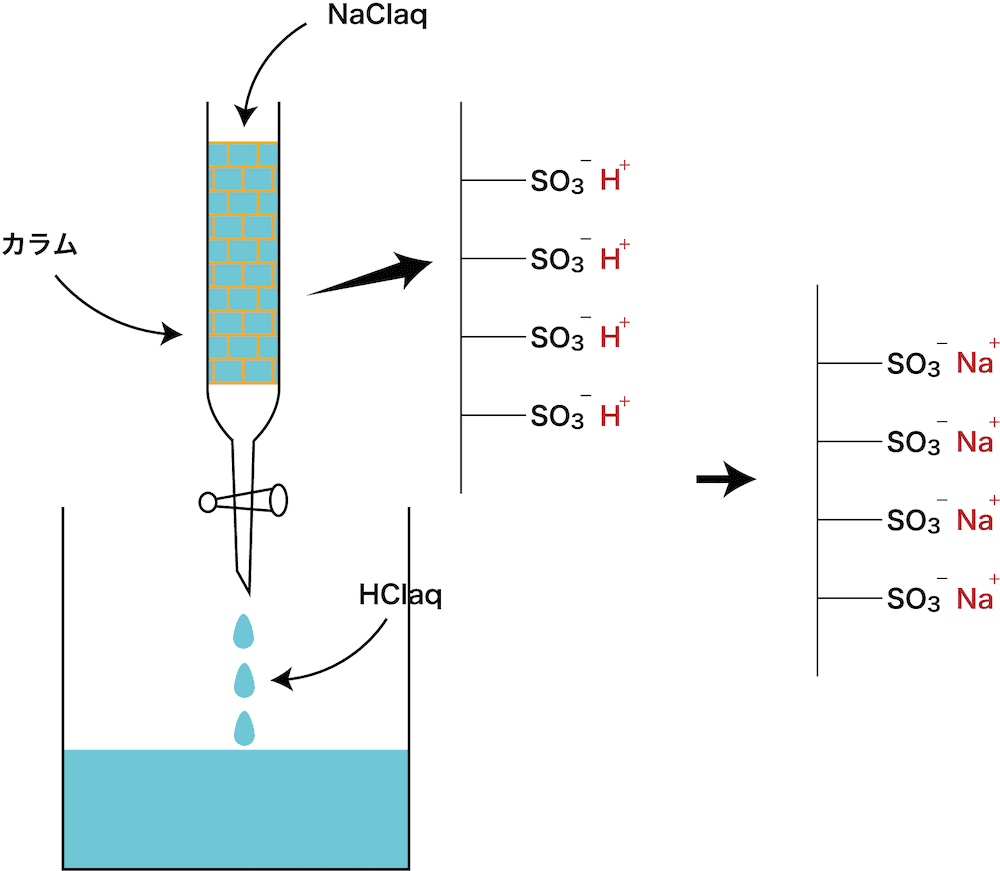
- 式で表すと次のようになる。
\[ \mathrm{R-SO_{3}^{-}H^{+}+Na^{+}Cl^{-}⇄R-SO_{3}^{-}Na^{+}+H^{+}Cl^{-}・・・① }\]
陰イオン交換樹脂
- 陰イオン交換樹脂(R-N+(CH3)3OHー)を詰めたカラムにNaCl水溶液を流す。
- 結果、水溶液中のClーが陰イオン交換樹脂中のOHーと置き換わって、下から水酸化ナトリウムNaOH水溶液が出てくる。
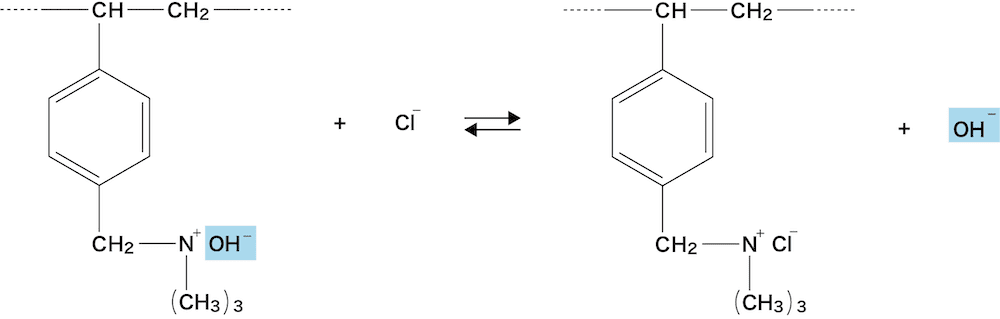
\[ \mathrm{R-N^{+}(CH_{3})_{3}OH^{-}+Na^{+}Cl^{-}⇄R-N^{+}(CH_{3})_{3}Cl^{-}+Na^{+}OH^{-}・・・②} \]
- 使用後の陽イオン・陰イオン交換樹脂は、塩酸や水酸化ナトリウム水溶液を加えることで①・②の反応を左向きに進めて、再生することができる。